超臨界水に関して
超臨界水とは
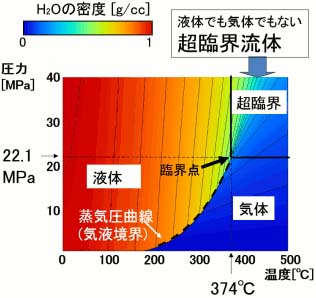
超臨界流体とは、気体と液体が共存できる限界の温度・圧力(臨界点)を超えた状態にあり、通常の気体、液体とは異なる性質を示すユニークな流体です。超臨界水・超臨界H₂Oは、22.1MPa以上の圧力、 374℃以上の温度で超臨界状態になります。
(右状態図を参照下さい)
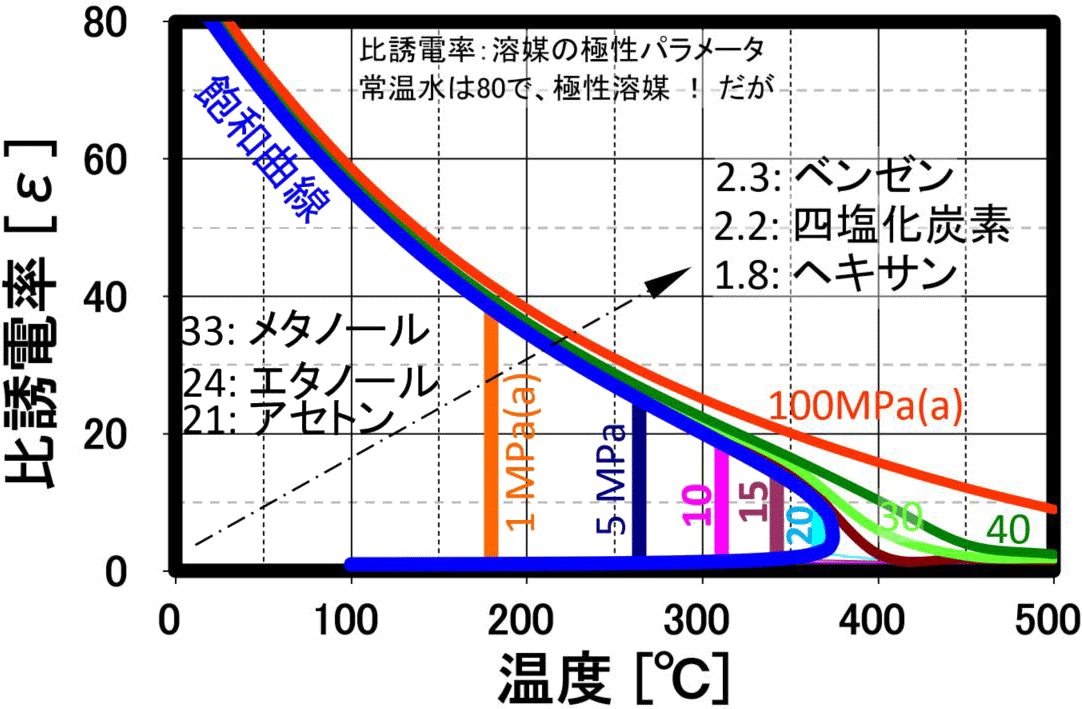
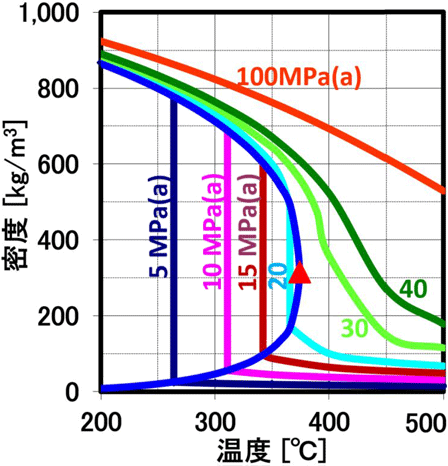
水分子は、常温付近では、70%の水分子が4つの水分子と水素結合し、氷と同じ結晶構造である4配位座の四面体を形成し、残り30%は、水素結合数が3以下で結晶構造をなし得ないので、全体として流体化しています。 温度が上昇すると、分子の運動が活発になり、4配位座の四面体構造は直線的に減少し、水の特異性が少なくなります。以下のQ8に示し特徴がありますが、高圧水の状態で温度を上げていくと、右図に示すように 誘電率とイオン積が大きく減少し、200℃以上の温度領域の亜臨界水の状態でも、イオン積が大きく増加し、加水分解反応が起こりやすくなり、 誘電率もエタノールなどと同程度以下になる超ユニークな特徴を示します。
超臨界水とは?の ページも参照下さい !
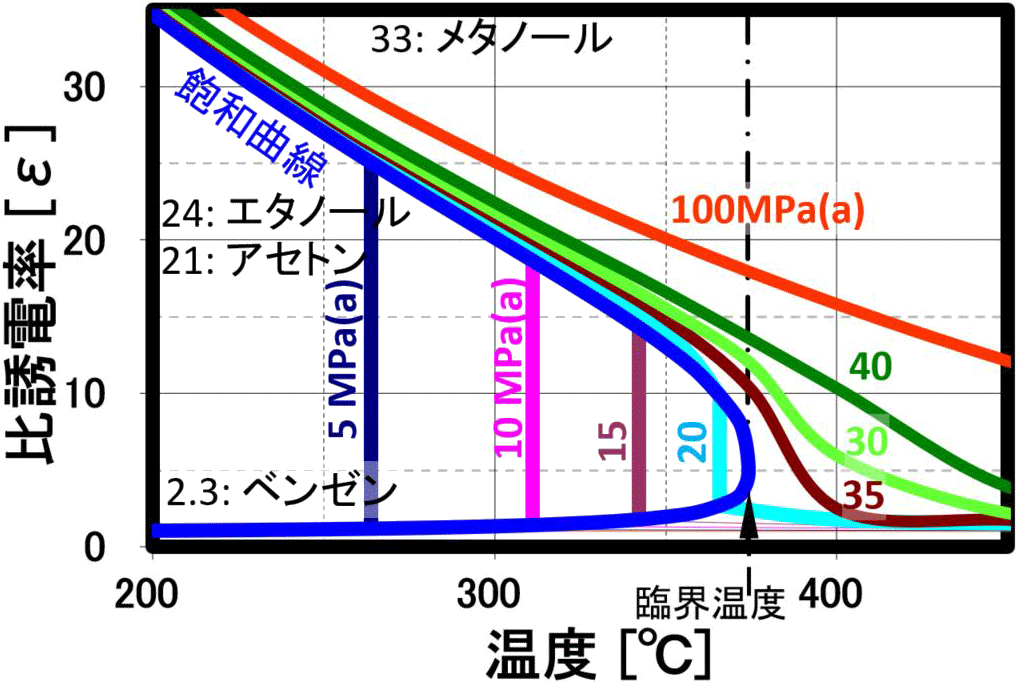
誘電率
溶媒の極性を評価するパラメータとして使用され、高圧水は温度の上昇と共に、上左図に示しように誘電率が大幅に低下します。 このため、20℃時に誘電率80の極性溶媒である水が温度上昇と共に、200℃近辺でメタノールやエタノール、300℃ではアセトンと同等の誘電率になります。更に温度を上げるとヘキサン等の一桁の誘電率を示し、臨界点付近では、無極性の有機溶媒である クロロホルムやエチルエーテルと同程度まで下がり、無極性溶媒として作用します。 臨界点近傍では、弱極性溶媒なみの誘電率で従来の有機溶媒に匹敵する溶解力が期待され、 実際に水と油が均一相になることが確認されています。経験則として、高極性物質は高極性溶媒に溶けやすく、低極性物質は低極性溶媒に溶けやすい、これは、似た物に溶けやすいと言い表わされる例ですが、温度と圧力により、 極性を変化させることができるのが、亜臨界水・超臨界水です。ベンゼン、トルエンなどが、臨界圧力・臨界温度以下で水と相溶・均一相を形成することが報告されています。
解離定数 (イオン積)
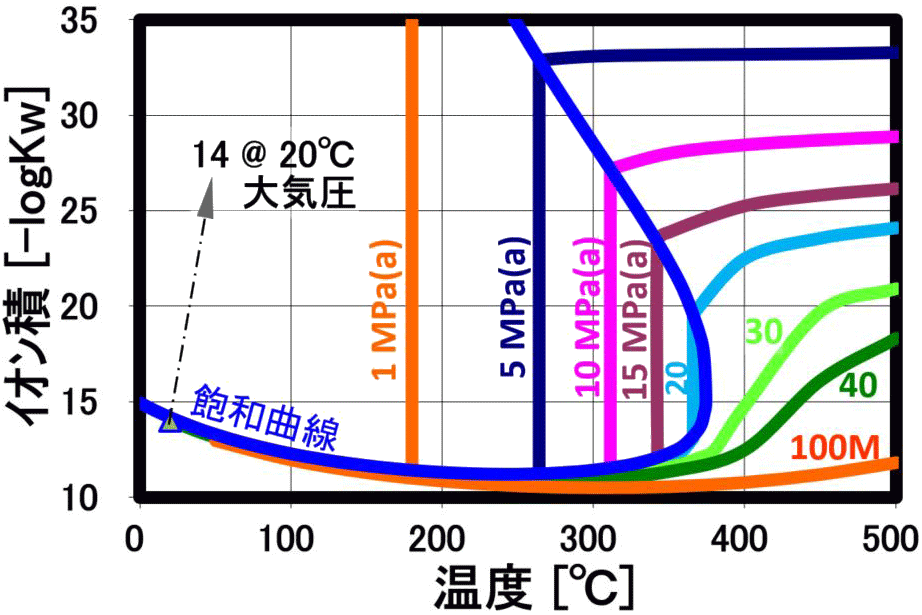
水の解離定数Kwは、20℃で10⁻¹⁴(mol/kg)²で、pHなど水溶液系の化学特性のベースになっていますが、 高圧水は、温度の上昇と共に、イオン積が大幅に増加します(上右図の縦軸は、-logKwで、イオン積増大で数値が小さくなります)。このため、電解質溶媒としてイオン反応(加水分解反応)に好都合な反応場を提供 すると共に制御できる溶媒として利用されています。解離が進み、水自体が酸やアルカリの機能を示し、加水分解作用が大きくなります。
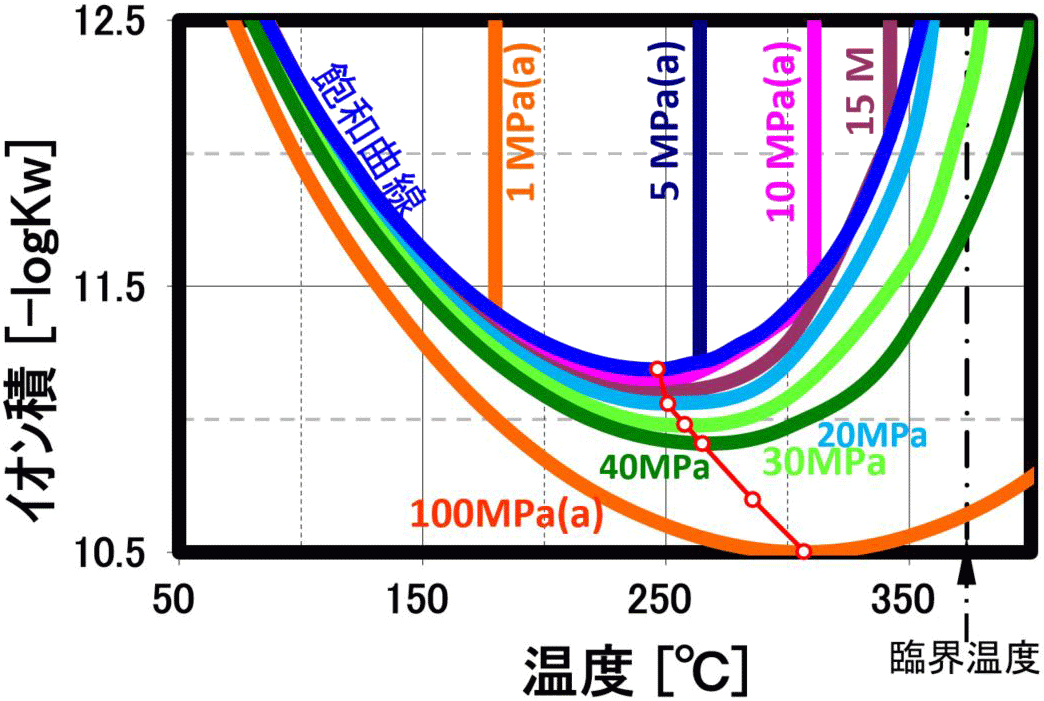
このイオン積は、250℃近辺で最大値 (図は-logのため最小値)を示し、高圧になると共にその最大値を示す温度は300℃に近づきます(上右下図の赤〇線は極大値軌跡を示します)。 更に温度を上げるとイオン積は急激に小さくなり、ガス的性質が強くなります。このため、縮重合物の加水分解反応を行う場合には、250℃近辺で、圧力は10MPa程度で行うのが、効率的になります。 即ち、この観点では、超臨界水よりも亜臨界水の方が反応特性が良い結果になります。
(常温の水は -log(Kw)=14、250℃の高圧水は -log(Kw)=11となり、 [H⁺]・[OH⁻]が1,000倍増加!) イオン積の最大値よりも、更に温度上昇させると、密度低下によりイオン積が減少しますが、逆にこの領域ではラジカル反応が支配的になります。この時、 超臨界水のような高密度の不活性物質が存在する事で、ラジカル反応でも反応経路や生成物分布の制御が期待されます。
受託試験 関係
御立会は、もちろん可能です。次のような委託試験も行っております。詳細はお試し試験事例、下記のQ6を参照下さい。
亜臨界水(高圧熱水)や超臨界水場を利用して、加水分解、脱水反応を瞬時に行うことで、通常では作製が困難なナノ粒子を瞬時に合成したり、有機無機ハイブリッド粒子といった表面修飾も可能です。バッチ式に加えて、流通式で、連続反応および連続回収も可能です。
標準仕様では、圧力 30MPa、温度 450℃での試験が可能です。カスタマイズすることで、27MPa、600℃の試験も可能です。
亜臨界水(高圧熱水)・超臨界水は上記のA0のイオン積の項で記載したように、pH(水素イオン指数)値は、右図に示しように 温度・圧力の上昇で減少し、最小値を示した後、増加します。右図は水の解離特性をpHで表したもので、飽和蒸気圧条件の250℃では、水のpHは、5.6 (但し、中性)となり、水素濃度としては常温の30倍に増加します。その後、昇温と共にpHは増加し、臨界点では 約8になり、これは、常温のメタノールと同程度の値です。
このように、水のpHは中性ですが、水素イオン濃度pH値は、大きく変わるため、常温での高・低pH値の薬液を高圧熱水と混合させる場合には、高温での強腐食環境下も含めて、 ステンレス製試験装置で使用可能かどうかの確認が必要ですので、右バナーよりお問合せをお願いします
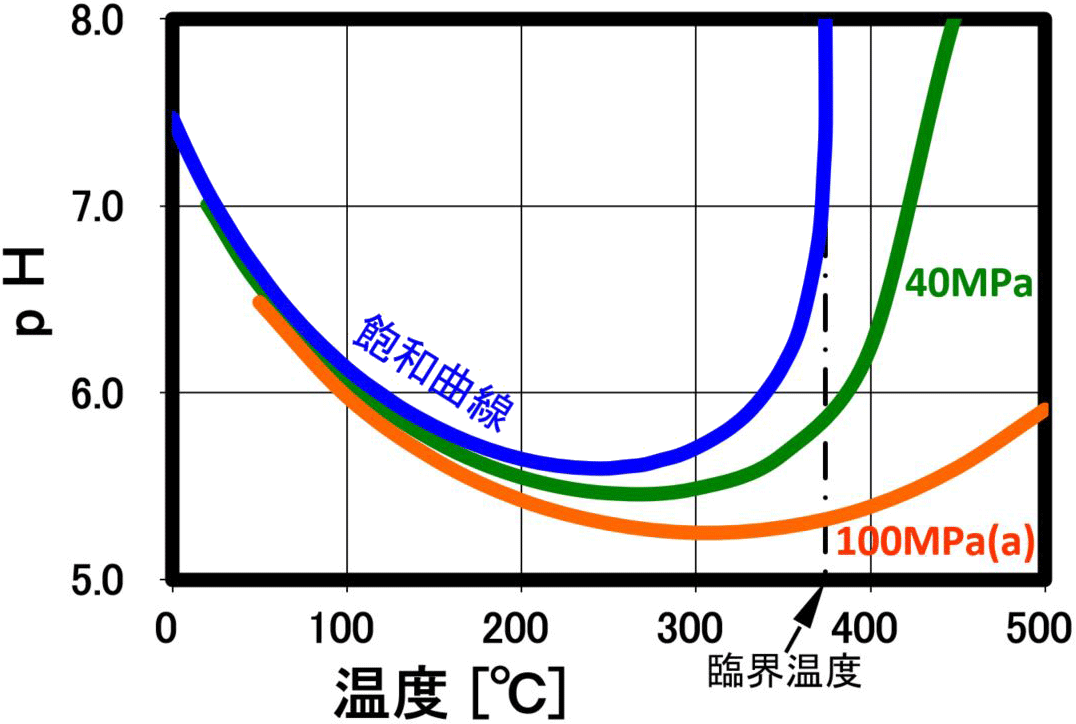
可能です。
水の場合は、超臨界よりも温度・圧力条件が緩やかな亜臨界/高圧熱水でその特徴が発揮できる場合がありますので、上記Q2の範囲内であれば、温度と圧力をコントロール可能ですので、フレキシブルな試験が可能な場合があります。 詳細はこちらのお試し試験事例を参照頂くか、右バナーよりお問合せ下さい。
可能です。
水以外に、ソルボサーマルや超臨界アルコールなどの試験も可能です。また、炭酸ガスCO₂を混合しての試験も行うことができます。炭酸ガスは、30MPaで、360℃以上で水と均一相・相溶を形成するとの報告があります。
以下の試験装置が使用可能です。
超臨界水ナノ粒子合成試験機
MOMI超®mini
最高使用圧力 30MPa、450℃、600cc-水/Hr
金属塩水溶液を高温水と混合することにより、加水分解と脱水反応により微粒子を合成できます。
また、粒子をスラリー投入することにより、その表面に有機基を修飾する事が可能です。
サンブル量は、原料濃度にもよりますが、本試験装置で、2~3g/Hr程度が可能です。

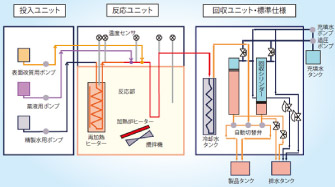
バッチ試験装置
30MPa、400℃、50ml(φ19)、圧力調節機能付きも使用可能です。
スラリー投入装置
プランジャーポンプで送液できないスラリーや高粘度液体を送液する装置で、スラリーが沈殿しないようにスターラーを備えています。試験機用のシングルシリンダ方式(右写真:30MPa、~10ml/min)、 間断の無い送液が可能なダブルシリンダ方式(30MPa、~100ml/min)があります。また、バイオマス、および磁性粒子を送液する場合は、強制撹拌方式を用いた装置を使用しますので、ご相談ください。

上記の試験装置を使用して行えるものであれば、基本、フレキシブルに何でも試験が可能です。代表的な例として、以下があります。
- ナノ粒子合成(急速昇温・緩速昇温)、有機修飾 他
- 長時間バッチ試験、亜・超臨界混合反応試験(緩速昇温)、高圧熱水反応系への気体導入試験(緩速昇温) 他
- 材料腐食試験、材料表面処理試験、廃棄物処理試験 他
用途・分野
以下の分野で適用・使用されている、或いは、適用可能性があります。
亜臨界水(高圧熱水)・超臨界水の適用分野の例
| 微粒子製造 ナノ粒子 合成反応 |
a) 金属酸化物の水熱合成・ナノ粒子:下記のQ9を参照下さい チタン酸バリウム BaTiO₃、ジルコニア ZrO₂、酸化セリウム CeO₃、光学材料(TiO₂、ZnO、ITO) 他 b) 有機・無機ハイブリッド微粒子(無機粒子表面への有機修飾):下記のQ10を参照下さい オレイン酸修飾コバルトブルーナナノ粒子、グラフェン、熱伝導フィラー表面処理 他 |
| リサイクル | a) 有機高分子のケミカルリサイクル: 脱水縮合化合物をモノマーなどに変換。下記のQ11を参照下さい b) その他のリサイクル: ・木質資源のリサイクル下記のQ11を参照下さい ・塩素系溶剤などの燃料転換、CFRPからの炭素繊維の回収 他 |
| 分解 | a) 超臨界水酸化分解: 酸素ガスとの相溶状態でPCB、ダイオキシン等の有害・有機塩素系化合物を定量下限値以下に分解。 b) 軽質化: 高粘度オイルサンド、超重質油などの軽質化によるパイプライン流動輸送化下記のQ12を参照下さい c) ガス化: バイオマス・有機系廃棄物から燃料ガスなどへの転換 他 |
ジルコニアナノ粒子 ZrO₂ : 一次粒子径が10nm以下の微粒子粉末で、主な結晶構造は正方晶、二次粒子径は19nmの球状粒子
オレイン酸修飾コバルトブルーナナノ粒子 CoAl₂O₄ : 表面が有機分子で覆われているため有機材料と親和性が高く、ポリマーに均一に混合するとの報告があります (20200413 accessed at https://www.wpi-aimr.tohoku.ac.jp/ajiri_labo/research/research_002.html)
H₂O 水は、地球上に最も豊富に存在する物質ですが、多くの物資に比べて非常に特異な物性を示します。例えば、a) 熱容量が大きいので熱媒体に適する、b) 分子量が小さい割には常温で液体、c) 誘電率が大きく(比誘電率80)、 電解質を良く溶解する、d) 水自体も一部解離している、これらは、水分子が酸素を中心に二つの水素が104.3°の角度で結合しているため、極性が強く、水分子間の水素と酸素の間が水素結合が形成され、実質的な分子量が相当大きくなって いる事に起因しているようです。上記のQ0も参照下さい。
この水を加圧下で温度を上げていくと、Q0に示すように誘電率とイオン積が大きく変化し、常温の水とは全く異なる性質を示し、従来と異なる材料創成などが可能になります。特に、超臨界水のもつ大きな特徴の一つである、 油のような有機溶媒と混ざりやすくなる性質が、化学反応や材料合成において,大きなメリットを発現します。通常,水中にしか溶けない物質と有機溶媒中にしか溶けない物質を反応させようとしても両者が 混合しないため,特殊な触媒を用いる必要がありました。しかし,超臨界状態では両者が完全に混じり合うため,触媒を用いることなく温度,圧力の操作で反応を進行させることが可能となります。
その大きな特徴、メリットは、以下の通りです。
| 自然溶媒 ◆ 処理後の易溶媒除去 |
◆ 物性制御が可能 | ◆ 高反応性(高温) | ◆ 気体と液体の両特徴 |
| ・誘電率(溶媒特性。親和性)可変 ⇒ 有極性から無極性まで ⇒ 水と有機物が均一相を形成! ・イオン積可変 ⇒ [H⁺]・[OH⁻]が1,000倍増加 ! ⇒ 加水分解反応、更に高温でラジカル反応 ・密度可変 |
・複合金属生成 ・粒子生成と有機修飾が同一場で反応 ⇒ 表面有機修飾ナノ粒子合成 ⬇ ナノ粒子は、 有機溶媒・樹脂などと ①均一分散、②高濃度分散、 ③低粘度化! |
・低分子・低粘性 ・低界面張力 ・高拡散/高浸透性 ・密度ゆらぎ・クラスタリング |
金属塩水溶液を加熱すると平衡は以下のように水酸化物、酸化物側にシフトします。水熱合成反応は、加水分解と脱水反応と考えることができます。この平衡のシフトを利用して(水)酸化物を合成する手法が水熱合成です。
MAx + xH₂O = M(OH)x + xHA、M(OH)x = MOx/2 + x/2H₂O
ここでAは、Cl⁻、NO₃⁻、SO₄⁻のようなアニオンです。
以下に代表的な超臨界水熱合成のナノ粒子の例を参考として示します。
| 出発物資 | ナノ粒子 | 粒子径 [nm] |
温度 [℃] |
圧力 [MPa] |
形態 |
| Al(NO₃)₃ | AlOOH | 50~600 | 250~400 | 25~40 | 六角板 |
| Ce(NO₃)₃ | CeO₂ | 20~300 | 250~400 | 30 | 八面体 |
| Co(NO₃)₃ | Co₃O₄ | ~100 | 400 | 35 | 八面体 |
| Fe(NO₃)₃ | α-Fe₂O₃ | ~50 | 400 | 35 | 球状 |
| Gd(NO₃)₂ | Gd(OH)₃ | ~20 | – | – | |
| Ni(NO₃)₂ | NiO | ~200 | 400 | 35 | 八面体 |
| 酢酸Ni(Ⅱ)+H₂ | Ni | ~500 | – | – | |
| Ti(SO₄)₂ | TiO₂ | ~20 | 400 | 35 | 球状 |
| Zn(NO₃)₂ | ZnO | ~20 | – | – | |
| ZrOCl₂ | ZrO₂ | ~10 | 400~490 | 30 | 球状 |
| 出発物資 | ナノ粒子 | 粒子径 [nm] |
温度 [℃] |
圧力 [MPa] |
形態 |
| Fe(NH₄)₂H(C₆H₅O₇)₂ | Fe₃O₄ | ~50 | 400 | 35 | 球状 |
| Al(NO₃)₃,Co(NO₃)₂ | CoAl₂O₄ | ~10 | – | – | |
| Ba(NO₃)₂,Fe(NO₃)₃ | BaO₆Fe₂O₃ | 50~300 | 400 | 30 | |
| Ba(NO₃)₂,Ti(SO₄)₂ | BaTiO₃ | 50~1,000 | – | – | |
| 酢酸Co(Ⅱ),酢酸Fe(Ⅱ) | CoFe₂O₄ | 40~70 | 200~400 | 25 | |
| LiOH,Co(NO₃)₂ | LiCoO₂ | 50~1000 | 300~400 | 100 | |
| Li塩、リン酸塩 他 | LiFePO₄ | 350 | 450 | – | |
| LiOH,Mn(NO₃)₂,H₂O₃ | LiMnO₄ | 20~40 | 400 | 30 | |
| 酢酸Ni(Ⅱ),酢酸Fe(Ⅱ) | NiFe₂O₄ | 30~40 | 190~400 | 25 | |
| Fe(NO₃)₃、Sr(NO₃)₂ | SrFe₁₂O₁₉ | 200 | 400 | 30 |
主に以下の文献などを参考にしました。:Journal of the Soceity of Inorganic Matericals, Japan 12,429 (2005) 表1
高圧力の科学と技術 vol.20,3 (2010) Table 1、超臨界流体とナノテクノロジー、シーエムシー出版 p103表1 他
高圧熱水で反応させると、上記Q9で示すナノ粒子合成と、金属・金属酸化物表面の金属とカプロン酸などのカルボン酸(COOH)やオレイン酸が酸素を介して粒子表面で結合し、有機表面修飾が同時にできます。 これを応用すると以下のような事への適用が可能です。
形状制御/活性面制御
例えば、セリア (CeO₂) ナノ粒子の場合
a) 有機高分子が共存しない系 8面体ナノクリスタル / 表面は(111)面
b) 適量の有機高分子が共存する系 6面体ナノクリスタル(高活性結晶面にのみ有機分子が接合)、高活性な(100)面を形成。
c) 大量の有機高分子が共存する系 15面体のナノクリスタル
低粘度高濃度分散液
粒子径が異なる球形アルミナ・ナノ粒子で充填密度を上げ、有機修飾により80%以上充填率で、流動性を確保
→ 電子デバイスパッケージ用封止剤
放熱材料への応用としての熱伝導フィラー
有機修飾アルミナ Al₂O₃、有機修飾窒素ホウ素 BN、有機修飾窒素アルミニウム AlN
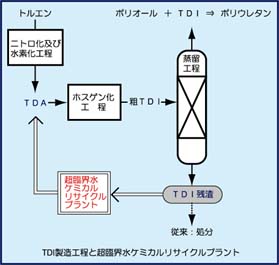
廃棄物のケミカル リサイクル プロセスの例として、ポリウレタン原料であるTDI(トリレンジイソシアネート)製造残渣から亜臨界水で加水分解させて TDA(トルエンジアミン)を回収し、再びTDIの原料として再利用するケミカルリサイクルプラントが1998年に千葉県鹿島で、世界で初めて稼働しました。本技術は、従来焼却処理していた残渣をアルカリ触媒等の添加剤を一切使用せず、 水だけを使用してケミカルルサイクルする非常に環境に優しい技術です。
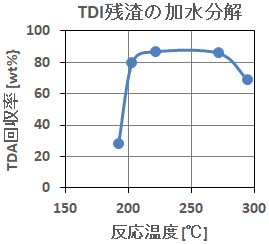
この技術は、上記Q0の解離定数(イオン積)で説明しているように、亜臨界水のイオン積が大幅に増加し、加水分解反応に好都合な反応場が提供された事により実現しました。右図に示すように、TDAの回収率は、 イオン積と相関関係がある結果となりました。10MPa、250℃、加水比 1.8wt=9mol、滞留時間10~20分の反応条件で、7,200 ton残渣/年の処理が実現しました。
同様に、2001年に韓国Namhae Chemical社で尿素からメラニン合成する際の残渣水中のアミド結合物(尿素、Ammeline、Ammelide、Biuret)をアンモニアに加水分解し、 尿素製造プロセスにリサイクルする3.4ton/日プラントが稼働しました。
また、ナイロン6製造工程から発生する蒸留残渣を18MPa、330℃、滞留時間20分、加水比2wtで加水分解すると、εカプロラクタムが80%以上の収率で回収される事が他社で確認されています。
以下の物質群にも加水分解によるケミカルリサイクルの適用が可能と考えられます。
| 化学結合 | ケミカルリサイクル適用可能な物質例 | |
|
エーテル結合 [ -O- ] |
樹脂 | ポリアセタール、変性ポリフェニレン、ケイ素樹脂 他 |
| 化学品 | エピクロヒドリン、ペンタエリスリトール、酸化プロピレン、ビスフェノールA 他 | |
| その他 | セルロース、キチン、キトサン 他 | |
|
エステル結合 [COO-] |
樹脂 | ポリエチレンテレフタレート(PET)、ポリウレタン、ポリカーボネイト、ポリブチレンテレフタレート、アルキド樹脂 他 |
| 化学品 | ジメチルテレフタレート、フレフタル酸、フタル酸ジブチル 他 | |
| アミド結合 [ -NH-C- ] || O |
樹脂 | ナイロン6、ナイロン66、尿素樹脂 他 |
| 化学品 | TDI、MDI、カプロラクタム、メラニン合成残渣(尿素、Biuret、Ammeline、Ammelide) 他 | |
| その他 | 絹 他 | |

上記Q11に示すリサイクルは、主に、イオン積が最大となる低温領域で利用されますが、分解する場合には、温度を更に上げて、ラジカル反応領域が利用されます。
高圧熱水中に酸素ガスを共存させて、有害物質を無害化する 超臨界水酸化分解法と、酸素ガスを使用せずに、単に高温でのラジカル反応による軽質化、ガス化があります。
酸素ガスを使用する超臨界酸化分解法は、SuperCriticla Water Oxidation略して、SCWOは、水の臨界温度374℃以上で高密度の水蒸気ですから、酸素と完全に混ざり合い、油も気体となっています。 このため、低い温度で水と油、酸素の気泡が混ざり合わない状態よりも、高速度で反応が進みます。これを利用し、PCB、ダイオキシンなどの難分解性有機塩素化合物などをほぼ完全に分解する技術として利用され、韓国Namhae Chemical社は、 2002年に爆薬(DNT/MNT)製造工程の廃液2m³/Hr、COD 50,000ppm、T-N(全窒素(Total nitrogen) 20,000ppmを各々40ppm、60ppm減少させるプラントを稼働させました。
日本国内でも以下の稼働プラントが稼働しました。
- 下水汚泥(含水率>90%)処理 : 1.1 m³/Hr、27MPa、~600℃ @ 兵庫県神戸市内, 1999年パイロット稼働
- 半導体製造廃液処理: 25MPa、~600℃ @ 千葉県館山市内, 1998年稼働
→ TMAH、アンモニア、TOCに対し、分解率は、99.9%以上で、工場補給水として再使用可能。
軽質化・ガス化の例では、ポリプロピレン PP を超臨界水で30分処理した場合、分解率は 400℃で30%、415℃で70%、430℃で95%以上で、60分処理ではほぼ100%分解との報告があります。 この報告によると、PPは高温で溶融状態となり、溶融相中でポリマー主鎖がランダムな位置で熱分解を受け、ラジカル反応が開始されます。更にある分子サイズ以下の分解生成物は、超臨界水中に拡散溶解し、超臨界水相中でさらに主鎖切断、 水素引抜き、異性化、環化やラジカル同士の再結合などの反応が進み、オリゴマー程度まで分解が進んだ生成物は油相成分として残ります。PPの主鎖末端や側鎖が切断されたり、生成した油相成分が更に分解を受けるとガス成分が生成します。
超臨界水メタン発生プロセスとして、ナフサの主成分であるヘキサンを原料として、25MPa、380℃、加水比0.67で超臨界水反応を行うと、メタン CH₄ の回収率は、>78mol%が確認されました。
装置 関係
MOMI超®シリーズは、第一種圧力容器に該当しない装置として、設計・製作されていますので、届出などは不要です。
一定条件・容量を超える容器、ガスを使用する場合などは、第一種圧力容器、高圧ガス保安法に該当する場合もあります。
詳細は、お問合せ下さい。
全般
⇒ 他ページへ (作成中)
